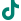海南普利制药股份有限公司(以下简称“普利制药”或“公司”)于近日收到了泰国食品药品监督管理局(FDA THAI)签发的盐酸多巴酚丁胺注射液(规格:250mg/20ml)的上市许可,标志着普利制药生产的盐酸多巴酚丁胺注射液具备了在泰国上市销售的资格。

盐酸多巴酚丁胺注射液泰国批件
中美双报,原料制剂一体化
作为普利制药中美双报的产品之一,盐酸多巴酚丁胺注射液此前已于2022年获得美国的上市许可,于2023年通过国家药监局一致性评价批准上市。
同时,盐酸多巴酚丁胺注射液属于普利制药的原料制剂一体化品种,其原料药已经成功完成中国CDE原料备案、美国DMF注册和欧盟CEP认证,稳定保障临床供应。

盐酸多巴酚丁胺原料分别在中国CDE、美国DMF、欧盟CEP备案/注册
普利制药泰国市场已布局多个产品
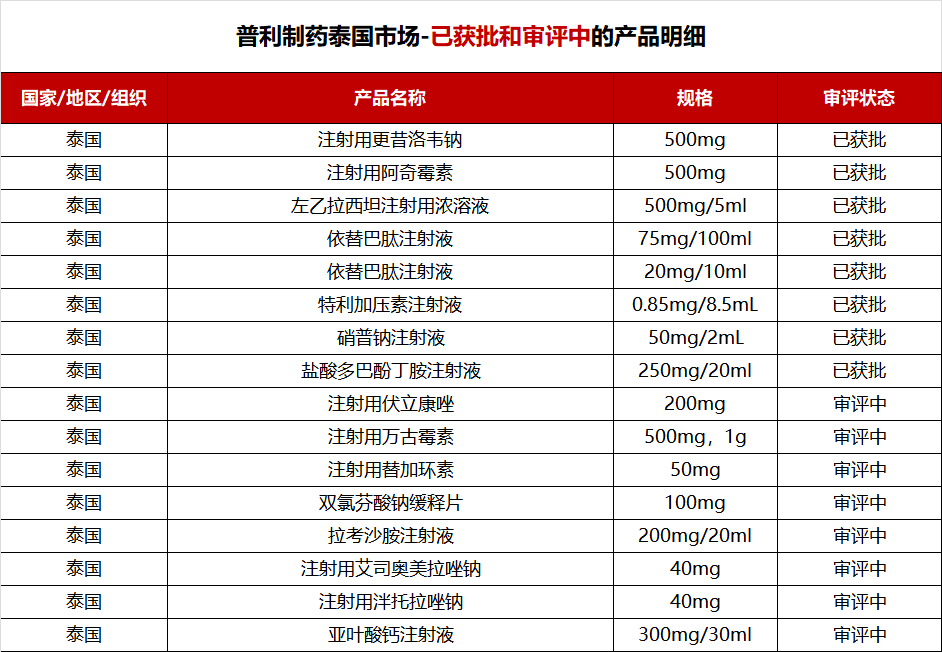
泰国是东盟成员国和创始国,位于东盟中心位置,是东盟第二大经济体。2023年泰国的GDP总量为5150亿美元,在东南亚地区排名第二。包括此次获批上市的盐酸多巴酚丁胺注射液,普利制药在泰国市场已有8个制剂产品获批、8个在审评中。
欢迎有兴趣海外拓展的同行,抱团出海;
也欢迎有志于国际发展的同仁加盟普利团队!
诚邀国际开拓的精英加盟,欢迎联系HR凌女士!
hnpolyhr@hnpoly.com

普利制药 1992 年成立于海口,是中国医药制剂国际化先导企业和国家工信部智能制造示范企业,已被国家工信部纳入工业转型升级中国制造 2025 年儿童药重点项目企业,2023年海南普利通过海关“AEO”高级认证。
此前,海南普利及其子公司浙江普利、安徽普利也曾多次顺利通过美国FDA、欧盟EMA现场审计。作为中国医药制剂国际化先导企业,普利制药多年来一直恪守全球较高质量标准,是国内为数不多的原料药和注射剂研发和生产平台,也是为数不多的同时获得美国、中国、欧盟等药监部门批准的原料药、关键辅料、药物药剂和GMP中间体CMO/CDMO的优质供应商。

 首页
首页